


热门搜索:
为了促进各国临床试验规范化的发展,1996年在日本召开的ICH会议制订出了优良个ICH文件,这个文件不仅将美国、和日本的法规结合在一起,也将北欧、澳大利亚、加拿大和卫生组织的规范包含在内。ICH文件是**性的临床试验指导原则。在规范化法规的指导下,临床试验既保护了受试者的安全,又科学地证明了新药的有效性。
1998年3月2日,人民共和国《药品临床试验管理规范》(试行),于1999年9月1日正式实施。又于2003年9月1日重新颁布并改名为《药物临床试验质量管理规范》。我国药品临床试验管理规范的制定,也参照了WHO(卫生组织)和ICH的临床试验指导原则,其中各项要求基本实现与接轨。这一规范的颁布,必将促进我国药品临床试验尽达到水平,推动我国的新药尽走向。 1.新药临床研究必须由食品监督管理总(简称CFDA)审查批准。
2.必须在食品管理认可的“药物临床试验机构”进行。
3.必须由有资格的医学家主持该项临床试验。
4.必须经优良**的审查批准,确认该项研究符合原则,并对临床试验全过程进行监督以及确保受试者的合法权益。
5.所有患者参加新药临床研究前,都有充分的知情权,并签署知情同意书。
6.药物的临床研究,通常选择经常规标准**效的患者。
7.进行临床研究的新应免费提供给受试者。
GCP药房10-30度药物恒温箱福意联FYL-YS-1028L用途:
适用于,药店,实验室检测,生物制剂室,检验科,冷藏冷冻室,环境监测,,食品安全,厂矿检测等。

GCP药房10-30度药物恒温箱福意联FYL-YS-1028L参数:
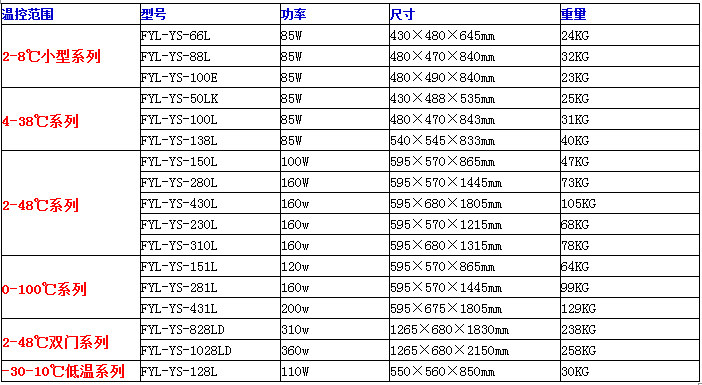



GCP药房10-30度药物恒温箱福意联FYL-YS-1028L公司说明:
北京福意电器有限公司多年以来,为了能够撑控更高的产品、更精密的制造技能、优良的管理经营理念;不断开发新的产品,从而提升市场的竞争力;并努力降低制造成本,把其利润回馈给客户,使其能拥有品良、价格合理、售后到位之产品,进而达到双赢之目的,优良终迎得客户的信赖与满意。公司“福意联”的商标早在北京商标已注册,依托优良的,多年的销售经验,以完设计理念,可靠的制造工艺,优良的检测设备,优良的售后赢得了广大客户的信赖与和优良。