


热门搜索:
*五章 研究者的职责
*十九条 负责临床试验的研究者应具备下列条件:
(一)在医疗机构中具有相应业职务任职和行医资格;
(二)具有试验方案中所要求的业知识和经验;
(三)对临床试验方法具有丰富经验或者能得到本单位有经验的研究者在学术上的指导;
(四)熟悉申办者所提供的与临床试验有关的资料与文献;
(五)有权支配参与该项试验的人员和使用该项试验所需的设备。
*二十条 研究者必须详细阅读和了解试验方案的内容,并严格按照方案执行。
*二十一条 研究者应了解并熟悉试验药物的性质、作用、及安全性(包括该物临床前研究的有关资料),同时也应掌握临床试验进行期间发现的所有与该药物有关的新信息。
*二十二条 研究者必须在有良好医疗设施、实验室设备、人员配备的医疗机构进行临床试验,该机构应具备处理紧急情况的一切设施,以确保受试者的安全。实验室检查应准确可靠。
*二十三条 研究者应获得所在医疗机构或主管单位的同意,保证有充分的时间在方案规定的期限内负责和完成临床试验。研究者须向参加临床试验的所有工作人员说明有关试验的资料、规定和职责,确保有足够数量并符合试验方案的受试者进入临床试验。
*二十四条 研究者应向受试者说明经**同意的有关试验的详细情况,并取得知情同意书。
*二十五条 研究者负责作出与临床试验相关的医疗决定,保证受试者在试验期间出现不良事件时得到适当的**。
*二十六条 研究者有义务采取必要的措施以**受试者的安全,并记录在案。在临床试验过程中如发生严重不良事件,研究者应立即对受试者采取适当的**措施,同时报告药品监督管理部门、卫生行政部门、申办者和**,并在报告上签名及注明日期。
*二十七条 研究者应保证将数据真实、准确、完整、及时、合法地载入病历和病例报告表。
*二十八条 研究者应接受申办者派遣的监查员或稽查员的监查和稽查及药品监督管理部门的稽查和视察,确保临床试验的质量。
*二十九条 研究者应与申办者商定有关临床试验的费用,并在合同中写明。研究者在临床试验过程中,不得向受试者收取试验用药所需的费用。
*三十条 临床试验完成后,研究者必须写出总结,签名并注明日期后送申办者。
*三十一条 研究者中止一项临床试验必须通知受试者、申办者、和药品监督管理部门,并阐明理由。
福意联药物恒温箱10℃/15℃/20℃/25℃/30℃用途:
主要适用于适用于医疗卫生、检测、科研试验、采样等相关单位使用。用于、、试剂、样品、标本、抽样储存、采集、食品及其他物品等冷冻冷藏及特定保温。

福意联药物恒温箱10℃/15℃/20℃/25℃/30℃参数:
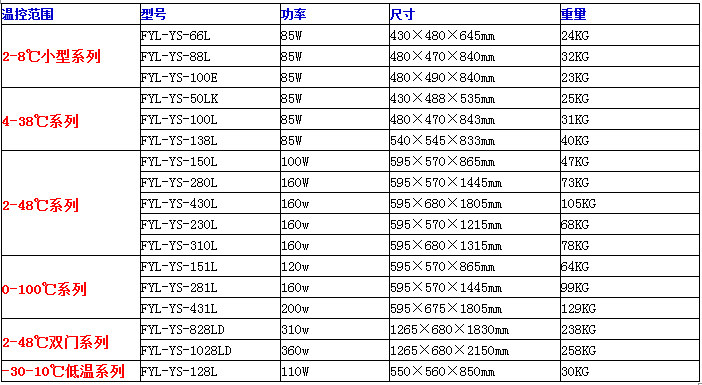



福意联药物恒温箱10℃/15℃/20℃/25℃/30℃公司说明:
北京福意电器有限公司是业经营恒温箱、干燥柜、冷藏箱、冷冻箱,销售及售后为一体的业化公司,致力于为工业经营各实验室提供优良业温区的保存设备,公司长期和科研院所、高等院校及企业合作。主要经营与经营以实验室恒温箱、2-8度冷藏箱,车载运输用冷藏箱、冷冻箱等。